аё•аёІаёЈаёІаёҮаёҳаёІаё•аёё аёЎаёөаёӣаёЈаё°а№ӮаёўаёҠаёҷа№Ңаёӯаёўа№ҲаёІаёҮаёЎаё«аёІаёЁаёІаёҘа№ҒаёҒа№ҲаёҷаёұаёҒаё§аёҙаё—аёўаёІаёЁаёІаёӘаё•аёЈа№Ңаё—аёөа№ҲаёЁаё¶аёҒаё©аёІа№ҖаёҒаёөа№Ҳаёўаё§аёҒаёұаёҡа№Ӯаё„аёЈаёҮаёӘаёЈа№үаёІаёҮаёӯаё°аё•аёӯаёЎа№ғаёҷаё•аёӯаёҷаё•а№үаёҷаё„аёЈаёҙаёӘаё•аёЁаё§аёЈаёЈаё©аёҷаёөа№ү а№ҖаёҠа№Ҳаёҷ аё—аёӯаёЎаёӣа№ҢаёӘаёұаёҷ,а№ҒаёӯаёӘаё•аёұаёҷ, аёЈаёұаё—а№Җаё—аёӯаёЈа№ҢаёҹаёӯаёЈа№Ңаё”, аёЎаёӯаёӘа№ҖаёҘаёўа№Ң, аёҡаёӯаё«а№ҢаёЈ аёҜаёҘаёҜ аёӘаёіаё«аёЈаёұаёҡаёӣаёЈаё°а№ӮаёўаёҠаёҷа№ҢаёӘаёІаёЎаёұаёҚа№ҖаёҠа№Ҳаёҷ аёӘаёіаё«аёЈаёұаёҡаёңаё№а№үаё—аёөа№Ҳа№ҖаёЈаёөаёўаёҷа№Җаё„аёЎаёөа№Җаёҡаё·а№үаёӯаёҮаё•а№үаёҷ аёҲаё°аёӣаёЈаёІаёҒаёҸаёҠаёұаё”а№ҖаёҲаёҷа№ҖаёЎаё·а№ҲаёӯаёЁаё¶аёҒаё©аёІа№ҖаёЈаё·а№ҲаёӯаёҮаёӘаёЎаёҡаёұаё•аёҙаё—аёІаёҮа№Җаё„аёЎаёөа№ҒаёҘаё°аёҒаёІаёўаё аёІаёһаёӮаёӯаёҮаёҳаёІаё•аёёаё•а№ҲаёІаёҮа№Ҷ а№ҖаёһаёЈаёІаё°аёҒаёІаёЈа№ҖаёӮа№үаёІа№ғаёҲа№ҖаёЈаё·а№ҲаёӯаёҮаё•аёІаёЈаёІаёҮаёҳаёІаё•аёёаёҲаё°аёҠа№Ҳаё§аёўа№ғаё«а№үа№ҖаёӮа№үаёІа№ғаёҲаё§аёҙаёҳаёөаёҒаёІаёЈаёЁаё¶аёҒаё©аёІаёӘаёЎаёҡаёұаё•аёҙаё”аёұаёҮаёҒаёҘа№ҲаёІаё§ аёҒаёІаёЈа№ғаёҠа№үаё•аёІаёЈаёІаёҮаёҳаёІаё•аёё ไดа№үаё–аё№аёҒаё•а№үаёӯаёҮаёҲаё°аёҠа№Ҳаё§аёўа№ғаё«а№үа№ҖаёӮа№үаёІа№ғаёҲаёӮа№үаёӯаёЎаё№аёҘаё•а№ҲаёІаёҮа№Ҷ аёӮаёӯаёҮаёҳาตุไดа№үаё”аёө а№ҒаёҘаё°аё—аёөа№ҲаёӘаёёаё”аёҒа№ҮаёҲаё°аёҲаё”аёҲำไดа№ү аёўаёҙа№ҲаёҮаёҒаё§а№ҲаёІаёҷаёұа№үаёҷаё•аёІаёЈаёІаёҮаёҳаёІаё•аёёаёҲаё°аё—аёіа№ғаё«а№үаёӘаёІаёЎаёІаёЈаё–аё—аёіаёҷаёІаёўаёӘаёЎаёҡаёұаё•аёҙаё—аёІаёҮа№Җаё„аёЎаёөаёӮаёӯаёҮаёҳาตุไดа№үа№ҖаёһаёЈаёІаё°аёңаё№а№үаё—аёөа№Ҳа№ғаёҠа№үаё•аёІаёЈаёІаёҮаёҳาตุไดа№үаё–аё№аёҒаё•а№үаёӯаёҮаёҲаё°аёӘаёІаёЎаёІаёЈаё–аё—аёіаёҷายไดа№үаё§а№ҲаёІаёҳаёІаё•аёёаё«аёҷаё¶а№ҲаёҮ аё„аё§аёЈаёҲаё°аёЎаёөаёӘаёЎаёҡаёұаё•аёҙаё„аёҘа№үаёІаёўаё„аёҘаё¶аёҮаёҒаёұаёҡаёҳаёІаё•аёёа№ғаё” а№ҒаёҘаё°аё–а№үаёІаёҳаёІаё•аёёаёЎаёөаёӘаёЎаёҡаёұаё•аёҙаё„аёҘа№үаёІаёўаёҒаёұаёҷа№ҒаёҘа№үаё§ аёӘаёІаёЈаёӣаёЈаё°аёҒаёӯаёҡаёӣаёЈаё°а№Җаё аё—а№Җаё”аёөаёўаё§аёҒаёұаёҷаёӮаёӯаёҮаёҳаёІаё•аёёа№Җаё«аёҘа№ҲаёІаёҷаёұа№үаёҷаёҒа№Үаёҷа№ҲаёІаёҲаё°аёЎаёөаёӘаёЎаёҡаёұаё•аё·а№ғаёҷаё—аёіаёҷаёӯаёҮа№Җаё”аёөаёўаё§аёҒаёұаёҷа№ҖаёҠа№Ҳаёҷ NaCl аёЎаёөаёӘаёЎаёҡаёұаё•аёҙаёӘа№Ҳаё§аёҷа№ғаё«аёҚа№Ҳаё„аёҘа№үаёІаёў KCl, RbCl, а№ҖаёһаёЈаёІаё° Na, K а№ҒаёҘаё° Rb аё•а№ҲаёІаёҮаёҒа№Үаёӯаёўаё№а№Ҳа№ғаёҷаё«аёЎаё№а№Ҳ IA аё«аёЈаё·аёӯ аёҳаёІаё•аёёаё—аёөа№Ҳ 104 ( Rf ) а№ҒаёҘаё° 105 (Ha)аёӢаё¶а№ҲаёҮа№Җаёӣа№ҮаёҷаёҳаёІаё•аёёаё—аёөа№ҲаёӘаёЈа№үаёІаёҮаёӮаё¶а№үаёҷаёЎаёөаёӘаёЎаёҡаёұаё•аёҙаё„аёҘа№үаёІаёўаёҒаёұаёҡ ( Hf )а№ҒаёҘаё° (Ta) аё•аёІаёЎаёҘаёіаё”аёұаёҡ а№ҒаёҘаё°а№ҖаёЎаё·а№ҲаёӯаёЁаё¶аёҒаё©аёІаё•аёІаёЈаёІаёҮаёҳаёІаё•аёёа№ғаё«а№үаёҘаё¶аёҒаёӢаё¶а№ҲаёҮаёўаёҙа№ҲаёҮаёӮаё¶а№үаёҷаёҒа№ҮаёҲаё°аёһаёҡаё§а№ҲаёІаёҷаёӯаёҒаёҲаёІаёҒаёҲаё°аёӘаёІаёЎаёІаёЈаё–аёЈаё°аёҡุไดа№үаё§а№ҲаёІаёҳаёІаё•аёёа№ғаё”аё«аёЈаё·аёӯаёӘаёІаёЈаёӣаёЈаё°аёҒаёӯаёҡаёӮаёӯаёҮаёҳаёІаё•аёёа№ғаё”аёҲаё°аёЎаёөаёӘаёЎаёҡаёұаё•аёҙаё„аёҘа№үаёІаёўаёҒаёұаёҡаёҳаёІаё•аёёаё«аёЈаё·аёӯаёӘаёІаёЈаёӣаёЈаё°аёҒаёӯаёҡаёӮаёӯаёҮаёҳаёІаё•аёёаё«аёҷаё¶а№ҲаёҮа№ҒаёҘа№үаё§аёҒа№ҮаёўаёұаёҮаёЈаё°аёҡุไดа№үаёӯаёөаёҒаё§а№ҲаёІаёҲаё°аёЎаёөаёӘаёЎаёҡаёұаё•аёҙа№ғаё”аёҡа№үаёІаёҮаё—аёөа№Ҳа№Ғаё•аёҒаё•а№ҲаёІаёҮаёҒаёұаёҷ а№ҖаёҠа№Ҳаёҷ ( H2SO4 ) а№ҒаёҘаё° ( H2TeO4 )а№ҒаёЎа№үаё§а№ҲаёІ S а№ҒаёҘаё° Te аёҲаё°аёӯаёўаё№а№Ҳа№ғаёҷаё«аёЎаё№а№Ҳ VIA аё”а№үаё§аёўаёҒаёұаёҷ а№Ғаё•а№ҲаёӘаёЎаёҡаёұаё•аёҙаёӮаёӯаёҮаёӘаёІаёЈаёӣаёЈаё°аёҒаёӯаёҡаё—аёұа№үаёҮаёӘаёӯаёҮаёЎаёөаё„аё§аёІаёЎа№Ғаё•аёҒаё•а№ҲаёІаёҮаёҒаёұаёҷаёӯаёўаё№а№Ҳ
аё•аёІаёЈаёІаёҮаёҳаёІаё•аёё
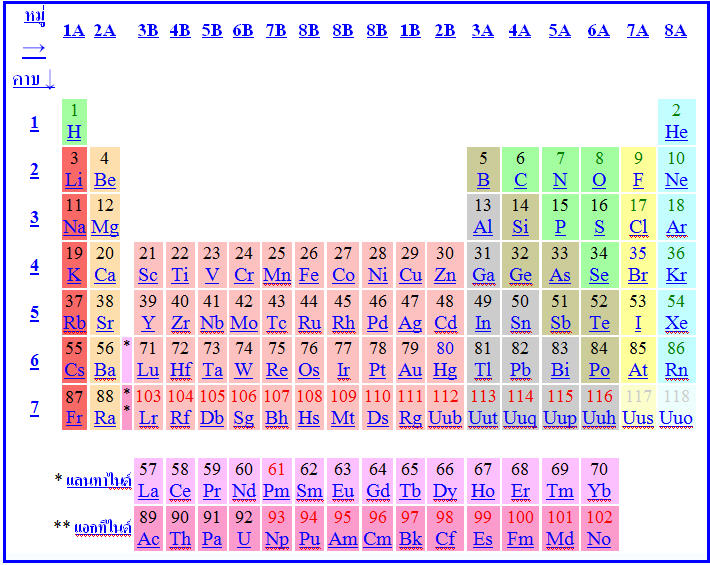
аё•аёІаёЈаёІаёҮаёҳаёІаё•аёё ( Periodic Table ) аё„аё·аёӯ аё•аёІаёЈаёІаёҮаё—аёөа№ҲаёЈаё§аёҡаёЈаё§аёЎаёҳаёІаё•аёёаё•а№ҲаёІаёҮ а№Ҷ а№ҖаёӮа№үаёІа№Җаёӣа№Үаёҷаё«аёЎаё§аё”аё«аёЎаё№а№Ҳ аё•аёІаёЎаё„аёёаё“аёӘаёЎаёҡаёұаё•аёҙаё—аёөа№Ҳа№Җаё«аёЎаё·аёӯаёҷ а№Ҷ аёҒаёұаёҷ ไวа№үа№Җаёӣа№Үаёҷаёһаё§аёҒа№Җаё”аёөаёўаё§аёҒаёұаёҷ а№Җаёһаё·а№ҲаёӯаёӘаё°аё”аё§аёҒа№ғаёҷаёҒаёІаёЈаёҲаё”аёҲаёіа№ҒаёҘаё°аёЁаё¶аёҒаё©аёІ
аёӘаёЎаёҡаёұаё•аёҙаёӮаёӯаёҮаёҳаёІаё•аёё
аёҳаёІаё•аёё (Element) аё„аё·аёӯ аёӘаёІаёЈаёҡаёЈаёҙаёӘаёёаё—аёҳаёҙа№Ңаё—аёөа№ҲаёӣаёЈаё°аёҒаёӯаёҡаё”а№үаё§аёўаёӯаё°аё•аёӯаёЎа№ҖаёһаёөаёўаёҮаёҠаёҷаёҙаё”а№Җаё”аёөаёўаё§ а№ҖаёҠа№Ҳаёҷ а№ӮаёӢа№Җаё”аёөаёўаёЎ (Na) а№ҒаёЎаёҒаёҷаёөа№ҖаёӢаёөаёўаёЎ (Mg) аё„аёІаёЈа№Ңаёҡаёӯаёҷ (C) аёӯаёӯаёҒаёӢаёҙа№ҖаёҲаёҷ (O) а№Җаёӣа№Үаёҷаё•а№үаёҷ
а№ғаёҷаёҒаёІаёЈаёҲаёұаё”аёҳаёІаё•аёёаёӯаёӯаёҒа№Җаёӣа№Үаёҷаё«аёЎаё§аё”аё«аёЎаё№а№ҲаёҲаё°аёӯаёІаёЁаёұаёўаёӘаёЎаёҡаёұаё•аёҙаё—аёөа№Ҳаё„аёҘа№үаёІаёўаё„аёҘаё¶аёҮаёҒаёұаёҷаёӮаёӯаёҮаёҳаёІаё•аёёа№Ғаё•а№ҲаёҘаё°аёҠаёҷаёҙаё”а№Җаёӣа№Үаёҷа№ҖаёҒаё“аё‘а№Ң а№ҖаёҠа№Ҳаёҷ а№ғаёҠа№үаё„аё§аёІаёЎа№Җаёӣа№Үаёҷа№ӮаёҘаё«аё°а№ҒаёҘаё°аёӯа№ӮаёҘаё«аё°а№Җаёӣа№Үаёҷа№ҖаёҒаё“аё‘а№Ң а№Ғаёҡа№ҲаёҮไดа№үа№Җаёӣа№Үаёҷ 3 аёҒаёҘаёёа№ҲаёЎ аё„аё·аёӯ а№ӮаёҘаё«аё° аёҒаё¶а№ҲаёҮа№ӮаёҘаё«аё° а№ҒаёҘаё°аёӯа№ӮаёҘаё«аё° а№ҒаёҘаё°аёўаёұаёҮаёӘаёІаёЎаёІаёЈаё–а№Ғаёҡа№ҲаёҮаёҳаёІаё•аёёаё—аёұа№үаёҮ 3 аёҒаёҘаёёа№ҲаёЎаёӯаёӯаёҒа№Җаёӣа№ҮаёҷаёҒаёҘаёёа№ҲаёЎаёўа№Ҳаёӯаёўа№Ҷไดа№үаёӯаёөаёҒ а№ҖаёҠа№Ҳаёҷ а№Ғаёҡа№ҲаёҮаёҒаёҘаёёа№ҲаёЎаёўа№Ҳаёӯаёўа№Ӯаё”аёўа№ғаёҠа№үаёӘаё–аёІаёҷаё°а№Җаёӣа№Үаёҷа№ҖаёҒаё“аё‘а№Ңаё„аё§аёІаёЎаё§а№ҲаёӯаёҮไวа№ғаёҷаёҒаёІаёЈа№ҖаёҒаёҙаё”аёӣаёҸаёҙаёҒаёҙаёЈаёҙаёўаёІ а№ҒаёҘаё°аёҘаёұаёҒаё©аё“аё°аё—аёөа№Ҳаёӯаёёаё“аё«аё аё№аёЎаёҙаёӣаёҒаё•аёҙ а№Җаёӣа№Үаёҷаё•а№үаёҷ аё”аёұаёҮа№Ғаёңаёҷаё аёІаёһа№ҖаёЈаёІа№Ғаёҡа№ҲаёҮаёҳаёІаё•аёёаёӯаёӯаёҒа№Җаёӣа№Үаёҷ 3 аёҠаёҷаёҙаё” аё„аё·аёӯ
- аёӯа№ӮаёҘаё«аё° ( Non-metal)
- аёҒаё¶а№ҲаёҮа№ӮаёҘаё«аё° ( Metalloid аё«аёЈаё·аёӯ Semi metal
аё«аёЎаё№а№Ҳаё•аёІаёЈаёІаёҮаёҳаёІаё•аёё
аё„аё·аёӯ аё„аёӯаёҘаёұаёЎаёҷа№Ңа№ғаёҷа№Ғаёҷаё§аё”аёҙа№ҲаёҮаёӮаёӯаёҮаёҳаёІаё•аёёа№Җаё„аёЎаёөа№ғаёҷаё•аёІаёЈаёІаёҮаёҳаёІаё•аёё аёЎаёөаё—аёұа№үаёҮаё«аёЎаё” 18 аё«аёЎаё№а№Ҳа№ғаёҷаё•аёІаёЈаёІаёҮаёҳаёІаё•аёёаёЎаёІаё•аёЈаёҗаёІаёҷа№ғаёҷаёўаёёаё„а№ғаё«аёЎа№Ҳаёҷаёөа№үаёҒаёІаёЈаёҲаёұаё”аё«аёЎаё§аё”аё«аёЎаё№а№ҲаёӮаёӯаёҮаёҳаёІаё•аёёа№ғаёҷаё•аёІаёЈаёІаёҮаёҳаёІаё•аёёаёҲаё°аёһаёҙаёҲаёІаёЈаё“аёІаёҲаёІаёҒаёҒаёІаёЈа№Ӯаё„аёҲаёЈаёӮаёӯаёҮаёӯаёҙа№ҖаёҘа№ҮаёҒаё•аёЈаёӯаёҷа№ғаёҷаё§аёҮа№Ӯаё„аёҲаёЈаёҠаёұа№үаёҷаёҷаёӯаёҒаёӘаёёаё”аёӮаёӯаёҮаёӯаё°аё•аёӯаёЎаёӢаё¶а№ҲаёҮаё„аёёаё“аёӘаёЎаёҡаёұаё•аёҙаё—аёІаёҮа№Җаё„аёЎаёөаёӮаёӯаёҮаёҳаёІаё•аёёаёҲаё°аёӮаё¶а№үаёҷаёӯаёўаё№а№ҲаёҒаёұаёҡаёҒаёІаёЈа№ғаё«а№үаёӯаёҙа№ҖаёҘа№ҮаёҒаё•аёЈаёӯаёҷаёҠаёұа№үаёҷаёҷаёӯаёҒаёӘаёёаё”аёҷаёөа№үаёҳаёІаё•аёёаё—аёөа№Ҳаёӯаё°аё•аёӯаёЎаёЎаёөаё§аёҮа№Ӯаё„аёҲаёЈаёӮаёӯаёҮаёӯаёҙа№ҖаёҘа№ҮаёҒаё•аёЈаёӯаёҷаёҠаёұа№үаёҷаёҷаёӯаёҒаёӘаёёаё”а№Җаё«аёЎаё·аёӯаёҷаёҒаёұаёҷаёЎаёұаёҒаёҲаё°аёЎаёөаё„аёёаё“аёӘаёЎаёҡаёұаё•аёҙаё—аёІаёҮа№Җаё„аёЎаёөа№ҒаёҘаё°аёҹаёҙаёӘаёҙаёҒаёӘа№Ңа№Җаё«аёЎаё·аёӯаёҷаёҒаёұаёҷ

- аё«аёЎаё№а№Ҳаё•аёІаёЈаёІаёҮаёҳаёІаё•аёёаёЎаёөаёЈаёІаёўаёҘаё°а№Җаёӯаёөаёўаё”аё”аёұаёҮаёҷаёөа№ү (а№ғаёҷаё§аёҮа№ҖаёҘа№Үаёҡа№Җаёӣа№ҮаёҷаёЈаё°аёҡаёҡа№ҖаёҒа№ҲаёІ: аёўаёёа№ӮаёЈаёӣ-аёӯа№ҖаёЎаёЈаёҙаёҒаёұаёҷ):
• аё«аёЎаё№а№Ҳ 1 (IA,IA): а№ӮаёҘаё«аё°а№ҒаёӯаёҘคาไаёҘ
• аё«аёЎаё№а№Ҳ 2 (IIA,IIA): а№ӮаёҘаё«аё°а№ҒаёӯаёҘคาไаёҘаёҷа№Ңа№ҖаёӯаёҙаёЈа№Ңаё—
• аё«аёЎаё№а№Ҳ 3 (IIIA,IIIB)
• аё«аёЎаё№а№Ҳ 4 (IVA,IVAB)
• аё«аёЎаё№а№Ҳ 5 (VA,VB)
• аё«аёЎаё№а№Ҳ 6 (VIA,VIB)
• аё«аёЎаё№а№Ҳ 7 (VIIA,VIIB)
• аё«аёЎаё№а№Ҳ 8 (VIII)
• аё«аёЎаё№а№Ҳ 9 (VIII)
• аё«аёЎаё№а№Ҳ 10 (VIII)
• аё«аёЎаё№а№Ҳ 11 (IB,IB): the а№ӮаёҘаё«аё°аё„аёӯаёўаёҷа№Ңа№ҖаёӯаёҲ (not a IUPAC-recommended name)
• аё«аёЎаё№а№Ҳ 12 (IIB,IIB)
• аё«аёЎаё№а№Ҳ 13 (IIIB,IIIA): аё«аёЎаё№а№Ҳа№ӮаёҡаёЈаёӯаёҷ
• аё«аёЎаё№а№Ҳ 14 (IVB,IVA): аё«аёЎаё№а№Ҳаё„аёІаёЈа№Ңаёҡаёӯаёҷ
• аё«аёЎаё№а№Ҳ 15 (VB,VA): аёһаёөаёҷаёҙаё„а№Ӯаё„а№ҖаёҲаёҷ (not a IUPAC-recommended name) or nitrogen group
• аё«аёЎаё№а№Ҳ 16 (VIB,VIA): а№ҒаёҠаёҘа№Ӯаё„а№ҖаёҲаёҷ
• аё«аёЎаё№а№Ҳ 17 (VIIB,VIIA): а№Ғаё®а№ӮаёҘа№ҖаёҲаёҷ
• аё«аёЎаё№а№Ҳ 18 (Group 0): аёҒа№ҠаёІаёӢаёЎаёөаё•аёЈаё°аёҒаё№аёҘ
аёӮаёӯаёӮаёӯаёҡаё„аёёаё“аёӮа№үаёӯаёЎаё№аёҘаёҲаёІаёҒ